1 Dengue epideemia taust: eskaleeruv ülemaailmne rahvatervise probleem
Dengue on äge sääskede levitatav viirushaigus, mida põhjustab dengue-viirus (DENV), mis on kujunenud maailmas kõige kiiremini levivaks arboviirushaiguseks, kujutades endast märkimisväärset ohtu rahvatervisele. Viimase kahe aastakümne jooksul on dengue-palaviku esinemissagedus maailmas dramaatiliselt suurenenud, kusjuures registreeritud juhtumite arv on alates 2021. aastast igal aastal kahekordistunud [1]. 2023. aasta detsembris kuulutas Maailma Terviseorganisatsioon (WHO) välja ülemaailmse dengue-palaviku hädaolukorra, et tugevdada koordineeritud rahvusvahelisi reageerimispüüdlusi. WHO epidemioloogilised hinnangud näitavad, et ligikaudu 3,9 miljardit inimest kogu maailmas on dengue-nakkuse ohus, kusjuures hinnanguliselt esineb igal aastal 390 miljonit nakatumist, millest 96 miljonit on kliiniliselt ilmsed juhtumid [1,2].
2 epidemioloogilist olulisemat sündmust
Denguepalaviku epidemioloogilisi omadusi kujundavad viroloogiliste tegurite, vektorökoloogia, peremeesorganismi immuunvastuste ja sotsiaal-keskkonnatingimuste koosmõju. Nende omaduste põhjalik mõistmine on oluline tõhusate ennetus- ja tõrjestrateegiate ning täpsete diagnostiliste lähenemisviiside väljatöötamiseks.
2.1 Edastusvektorid ja linnakeskkonna edastusmustrid
Dengue viirus levib peamiseltAedes aegypti ja Aedes albopictussääsed. Nende vektorliikide seas on Aedes aegypti tunnustatud kõige kriitilisema levikuvektorina, mida iseloomustab kõrge „inimese kohanemisvõime“ ja laialdane levik troopilises ja subtroopilises linnakeskkonnas. Erinevalt teistest arboviiruslike patogeenide sääsevektoritest on Aedes aegyptil järgmised peamised epidemioloogilised omadused:
Eelistus paljunemiseks inimtekkelistes keskkondades (nt veemahutid, kasutuselt kõrvaldatud rehvid)
- Inimese vere kui toitaineallika tugev tropism
-Päevane söömiskäitumine
Need tunnused määratlevad denguepalaviku tüüpiliseks haiguseks."Linna nakkushaigus"kusjuures tihedalt asustatud piirkondades on edastustõhusus oluliselt suurenenud. WHO-ga seotud uuringud on näidanud, et tiheda asustusega linnakeskkondades võib sääskede ja inimeste kokkupuute sagenemine oluliselt tõsta DENV baaspaljunemisarvu (R₀), kiirendades seeläbi epideemiate levikut [2].
2.2 Globaalsed levikutrendid ja neid mõjutavad tegurid
WHO aruannete kohaselt on dengue palaviku juhtumite arv maailmas viimase kahe aastakümne jooksul hüppeliselt suurenenud [1,3]. See kasvutrend on peamiselt tingitud järgmistest omavahel seotud teguritest:
(1) Kliimamuutused: Tõusvad globaalsed temperatuurid mitte ainult ei laienda sääskede vektoritele sobivate elupaikade geograafilist ulatust, vaid lühendavad ka DENV välist inkubatsiooniperioodi sääse peremeesorganismis, suurendades seeläbi ülekande efektiivsust. WHO on valideerinud kliimast tingitud sääskede tiheduse muutused usaldusväärseks denguepalaviku puhangute ajalis-ruumilise dünaamika ennustajaks.
(2) Linnastumine: kiire ja planeerimata linnade laienemine on loonud sääskede vektoritele arvukalt paljunemispaiku, samas kui suurenenud asustustihedus on tugevdanud DENV ülekandeahelate järjepidevust.
(3) Globaalne rahvastiku liikumine: rahvusvaheline reisimine ja kaubandus on soodustanud DENV kiiret piiriülest levikut, soodustades üleminekut imporditud juhtudest püsivale kohalikule levikule. WHO seireandmed näitavad, et aastatel 2010–2021 teatasid Ameerika Ühendriigid 7528 reisimisega seotud denguepalaviku juhtumist, millest 3135 vajasid haiglaravi ja 19 lõppesid surmaga.
(4) Vektorite leviku laienemine: Ülemaailmselt laieneb jätkuvalt Aedes aegypti ja Aedes albopictus geograafiline leviala ning Aedes sääsed on üha enam levinud Euroopa osades. Selle tulemusena on dengue palavik arenenud traditsiooniliselt piirkondlikust epideemiast ülemaailmseks rahvatervise ohuks.
2.3 Mitme serotüübi samaaegne ringlus ja taasnakatamise mehhanismid
Dengue viirus koosneb neljast antigeenselt erinevast serotüübist (DENV-1 kuni DENV-4). Ühe serotüübiga nakatumine annab selle konkreetse serotüübi vastu pikaajalise kaitsva immuunsuse, kuid ülejäänud kolme serotüübi vastu ainult ajutise ja osalise ristkaitse. Üldpopulatsioon on DENV suhtes universaalselt vastuvõtlik ning ainult osal nakatunud inimestel tekib kliiniline haigus [2].
Endeemilistes piirkondades ringleb sageli samaaegselt mitu DENV serotüüpi, mille tulemuseks on potentsiaal põdeda mitut denguepalavikuinfektsiooni kogu elu jooksul. WHO epidemioloogilised uuringud on tuvastanud mitme serotüübi samaaegse ringluse kui perioodiliste denguepalaviku puhangute peamise põhjustaja [1].
2.4 Teisene infektsioon ja antikehadest sõltuv võimendumine
Dengue epidemioloogias on kriitilise tähtsusega ja ainulaadne nähtusantikehadest sõltuv võimendus (ADE)Heteroloogilise DENV serotüübiga sekundaarse infektsiooni ajal hõlbustavad primaarse infektsiooni ajal toodetud mitteneutraliseerivad antikehad viiruse sisenemist monotsüütidesse ja makrofaagidesse, suurendades seeläbi viiruse replikatsiooni. WHO on seda mehhanismi laialdaselt tunnustanud kui peamist patogeenset tegurit raske denguepalaviku, sealhulgas dengue-hemorraagilise palaviku ja dengue-šoki sündroomi korral [1].
WHO epidemioloogilised andmed näitavad järjekindlalt, et sekundaarse denguepalaviku infektsiooniga inimestel on oluliselt suurem risk raske haiguse tekkeks võrreldes primaarse infektsiooniga inimestega – see omadus on haiguse jälgimise ja kliinilise ravi seisukohalt väga oluline. Oluline on märkida, et kuigi raske haiguse risk on sekundaarse infektsiooni ajal suurenenud, võib mis tahes DENV serotüübiga infektsioon potentsiaalselt progresseeruda raskeks denguepalavikuks [1].
2.5 Mittespetsiifilised kliinilised ilmingud ja valediagnoosimise risk
Dengue palaviku kliinilised ilmingud on märkimisväärselt mittespetsiifilised, eriti haiguse algstaadiumis, kattudes sageli teiste sääskede kaudu levivate viirusnakkuste (nt chikungunya ja Zika viirused) ning teatud hingamisteede infektsioonidega. WHO hinnangul on 40–80% DENV-nakkustest asümptomaatilised [3].
Tüüpiliste kliiniliste ilmingute hulka kuuluvad:
-Äge palavik (kestab 2–7 päeva, võib olla kahefaasiline)
-Tugev peavalu ja retroorbitaalne valu (valu silmade taga)
-Lihas- ja liigesevalu (mida tavaliselt nimetatakse ka "luumurrupalavikuks")
-Makulaarne või makulopapulaarne lööve
Kerged hemorraagilised ilmingud (nt ekhümoos, ninaverejooks, igemete veritsus)
Sümptomaatiline dengue jaguneb tavaliselt kolmeks erinevaks faasiks: palavikufaas, kriitiline faas ja taastumisfaas. Ligikaudu vähem kui 5% sümptomaatilistest patsientidest progresseerub raskeks denguepalavikuks. Spetsiifiliste kliiniliste tunnuste puudumise tõttu on ainult kliinilistel sümptomitel põhinev diagnoosimine keeruline, mis suurendab vale- ja aladiagnoosimise riski. WHO rõhutab selgesõnaliselt, et ainuüksi kliiniline diagnoos ei ole täpsuse tagamiseks piisav, mistõttu on laboratoorne kinnitus hädavajalik [1].
3 põhipunkti WHO dokumendist „Dengue-viiruse laboratoorne testimine: ajutised juhised, aprill 2025”
2025. aasta aprillis avaldas Maailma Terviseorganisatsioon ajakohastatud ajutised juhised DENV laboratoorsete testide kohta, pakkudes autoriteetseid tehnilisi juhiseid denguepalaviku diagnoosimiseks kogu maailmas. Need juhised sünteesivad uusimaid tõendeid dengue laboratoorsete testide kohta käimasoleva ülemaailmse denguepalaviku hädaolukorra kontekstis ja pakuvad praktilisi soovitusi, mis on kohandatud erineva ressursitasemega keskkondadele.

3.1 Testimisstrateegia põhiprintsiibid
Juhendis rõhutatakse, et denguepalaviku diagnoosimisel tuleb kasutada haiguse staadiumil põhinevat mitme markeriga kombineeritud testimisstrateegiat [1]. Kuna universaalne diagnostiline algoritm puudub, tuleks testimisstrateegiaid kohandada kohalike epidemioloogiliste oludega, võttes arvesse järgmisi võtmetegureid [1]:
-Nakkusstaadium: Sümptomite ilmnemisest möödunud päevade arv määrab sobivaima testimismeetodi.
-Proovi tüüp: täisvere, plasma või seerumi sobivus DENV tuvastamiseks
-Regionaalne epidemioloogia: lokaalselt levivad DENV serotüübid ja teiste arboviiruste kaasringlus
-Kaasinfektsiooni risk: Piirkondades, kus arboviiruse ringlus kattub, tuleks kaaluda mitmekordset testimist, et eristada erinevaid patogeene.
3.2 Etapipõhine testimisstrateegia
WHO juhiste kohaselt peaks denguepalaviku laboratoorne testimine toimuma selgete ajaraamide järgi, mis põhinevad haiguse staadiumil [1,2]:
(1) Ägeda faasi testimine (≤7 päeva pärast haigestumist)
-Nukleiinhappe testimine (molekulaarne testimine): pöördtranskriptsiooni-polümeraas-ahelreaktsioon (RT-PCR) ja muud molekulaarsed meetodid tuvastavad DENV RNA-d suure tundlikkusega.
-Antigeeni testimine: NS1 antigeeni tuvastamine, mis muutub tuvastatavaks 1-3 päeva jooksul pärast haigestumist.
Ägeda faasi ajal on vireemia tase suhteliselt kõrge ning nukleiinhapete ja antigeenide testimine saavutab optimaalse tundlikkuse.
(2) Taastumisfaasi testimine (≥4 päeva pärast haigestumist)
-Seroloogiline testimine: IgM antikehad muutuvad tavaliselt tuvastatavaks umbes 4. päeval pärast haiguse algust.
-Enamikul juhtudel püsivad IgM antikehad 14–20 päeva ja mõnel juhul võib püsivus ulatuda kuni 90 päevani.
IgG testimisel on ägeda denguepalaviku diagnoosimisel piiratud väärtus varasema flaviviiruse infektsiooni või vaktsineerimise tagajärjel tekkinud võimalike ristreaktiivsete antikehade tõttu.
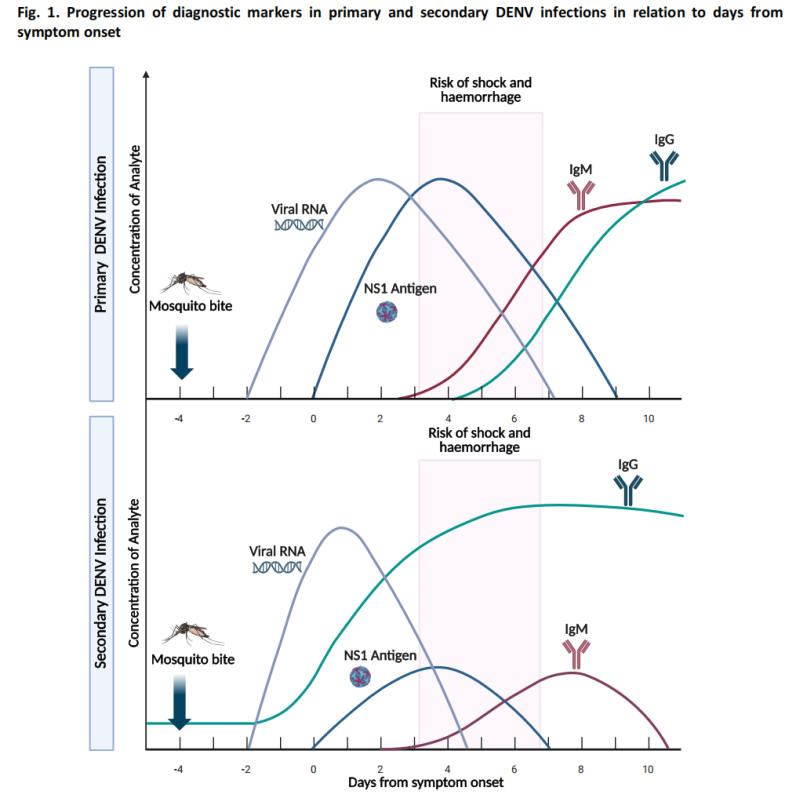
(3) Kahtlustatava juhtumi diagnostika algoritm
Juhend sisaldab kahtlustatava denguepalaviku juhtumite diagnostilist algoritmi, mis soovitab sobivaid testimismeetodeid sümptomite ilmnemisele järgnenud päevade arvu põhjal: varases faasis on peamised lähenemisviisid NS1 antigeeni testimine ja nukleiinhapete testimine, hilisemas faasis aga seroloogiline testimine.
3.3 Katsemeetodi toimivuse hindamine ja valik
WHO andmetel on erinevate denguepalaviku testimise tulemuslikkuse ja rakendatavate stsenaariumide süstemaatiline hindamine järgmine:
| Testimismeetod | Sihtmärk | Ajaaken | Peamine rakendusstsenaarium | Kaalutlused |
| Nukleiinhappe testimine | Viiruslik RNA | 1–7 päeva pärast haigestumist | Varajane kinnitus, serotüübi identifitseerimine | Kuldse standardmeetodi puhul on vaja spetsiaalset laborivarustust ja tehnilist oskusteavet. |
| NS1 antigeeni testimine | Mittestruktuurne valk | 1-3 päeva pärast algust | Varajane kiirsõeluuringu | Saadaval kiirdiagnostika testi (RDT) vormingus, sobib piiratud ressursiga keskkondadesse |
| IgM antikehade testimine | Spetsiifilised IgM antikehad | ≥4 päeva pärast haigestumist | Hiljutise infektsiooni diagnoosimine | Ainult üks seerumiproov viitab võimalikule hiljutisele infektsioonile; kinnitamiseks on vaja serokonversiooni. |
| IgG antikehade testimine | Spetsiifilised IgG antikehad | Paranemisstaadiumis/eelnev infektsioon | Epidemioloogiline uuring, immuunsuse seisundi hindamine | Üks seerumiproov ei sobi ägeda denguepalaviku diagnoosimiseks |
| Kombineeritud testimine (NS1+IgM/IgG) | Antigeen + antikehad | Täielik haiguse kulg | Denguepalaviku nakkuse põhjalik diagnoosimine | Praegu kõige paremini toimiv RDT-vorming denguepalaviku diagnoosimiseks |
| NGS | Viiruslik RNA | 1–7 päeva pärast haigestumist | Viiruse genoomne jälgimine | Nõuab spetsiaalseid sekveneerimisseadmeid ja bioinformaatilise analüüsi võimalusi |
4 Makro- ja mikrotesti denguepalaviku tuvastamise tootesoovitust stsenaariumide kaupa
Denguepalaviku ennetamise ja tõrje toetamiseks pakub Macro & Micro-Test integreeritud diagnostikaportfelli, mis hõlmab kiirsõeluuringuid, molekulaarset kinnitust ja genoomset seiret, rahuldades vajadusi puhangute ohjamise eri etappides.
4.1 Stsenaarium 1: Kiire sõeluuring ja sihipärane jälgimine
Kehtib palavikliinikute, esmatasandi tervishoiuasutuste, puhangute ajal kogukonnas tehtava sõeluuringu ja sadama-/piirikarantiini kohta.
-Dengue viiruse NS1 antigeeni kiirtest: tuvastab varajase nakkuse (1-3 päeva pärast haigestumist) ja annab 15-minutilise tulemuse kiireks triaažiks.
-Dengue viiruse IgM/IgG antikehade test: eristab primaarseid ja sekundaarseid infektsioone, et hinnata raske haiguse riski.
-Dengue viiruse NS1 antigeeni + IgM/IgG kombineeritud kiirtest: tuvastab samaaegselt antigeeni ja antikehi täielikuks diagnoosimiseks.
-Chikungunya viiruse IgM/IgG antikehade test: võimaldab diferentsiaaldiagnoosi denguepalavikuga, et patogeene täpselt tuvastada.
4.2 Stsenaarium 2: Täppisdiagnostika ja hädaolukorrale reageerimine
-Dengue viiruse I/II/III/IV nukleiinhappe tuvastamise komplekt: tuvastab ja eristab 4 serotüüpi (tuvastuspiir 500 koopiat/ml) puhangu jälgimiseks.
-Lüofiliseeritud dengueviiruse PCR-komplekt: toatemperatuuril transporditav, sobib piiratud ressurssidega piirkondadele ja äkiliste puhangute korral.
-Dengue/Zika/Chikungunya multipleksne reaalajas PCR-komplekt: tuvastab samaaegselt 3 arboviirust tõhusaks diferentsiaaldiagnoosiks keeruliste puhangute korral.

Kõik ülaltoodud reagendid ühilduvad AIO 800 täisautomaatse proovist vastuseni süsteemiga, vähendades käsitsi töötamist ja ristsaastumist ning parandades tõhusust ja bioohutust.
4.3 Stsenaarium 3: Genoomne jälgimine ja viirusliku liini analüüs
Kohaldatav riiklikele referentlaboritele ja rahvatervise uurimisasutustele, kooskõlas WHO NGS-i seisukohaga.
Macro & Micro-Testi genoomse seire lahendused toetavad viiruse jälgimiseks, ülekandeahela selgitamiseks, variantide jälgimiseks ja vaktsiinistrateegia kohandamiseks kogu genoomi sekveneerimist. Need toetavad käsitsi/automatiseeritud töövooge, parandades läbilaskevõimet ja reprodutseeritavust, võimaldades laboritel minna üle rutiinselt testimiselt täiustatud seirele, mis on kooskõlas WHO rõhuasetusega viirusliku evolutsiooni seire tugevdamisele.

4.4 Integreeritud lahenduste väärtus
Macro & Micro-Test pakub täielikke diagnostilisi lahendusi arboviiruste tuvastamiseks, toetades puhangu ohjamise iga etappi: kiirsõeluuringute tööriistu esmatasandi tervishoiuasutustele, molekulaarset kinnitust täppisdiagnoosimiseks ja kogu genoomi analüüsi võimalusi epidemioloogiliseks seireks. Tänu suure jõudlusega analüüsidele, paindlikele töövoogudele ja automatiseerimisvalmis platvormidele annavad need lahendused laboritele ja rahvatervise süsteemidele võimaluse tugevdada valmisolekut ja reageerimist tekkivatele arboviirusohtudele kogu maailmas.
Viited
[1] Maailma Terviseorganisatsioon. Dengue-viiruse laboratoorne testimine: ajutised juhised, aprill 2025. Genf: Maailma Terviseorganisatsioon; 2025.
[2] WHO ülemaailmse arboviiruse algatuse tehniline nõuanderühm. Ülemaailmse valmisoleku ja reageerimise tugevdamine arboviirusest tingitud haiguste ohtudele: üleskutse tegutseda. Lancet Infect Dis. 2026;26(1):15-17.
[3] Lancet Microbe. Dengue diagnostika dilemma ületamine. Lancet Microbe. 2025;6(7):101190.
Postituse aeg: 20. märts 2026
