Hiljuti avaldas British Journal of Clinical Pharmacology esimese kliinilise juhise, mille töötas välja Ühendkuningriigi farmakogenoomika regulatiivse teaduse ja innovatsiooni tippkeskus (CERSI PGx), pealkirjaga „CYP2C19 genotüübi testimine klopidogreeli puhul: Ühendkuningriigi farmakogenoomika regulatiivse teaduse ja innovatsiooni tippkeskuse (CERSI PGx) väljatöötatud juhend“. See oluline dokument keskendub CYP2C19 genotüüpimise kliinilisele väärtusele klopidogreeli ravi suunamisel.

CERSI PGx kohta
CERSI PGx on üks seitsmest Ühendkuningriigi valitsuse toetatud regulatiivse teaduse ja innovatsiooni keskusest, mis käivitati jaanuaris 2025. Keskust juhib Liverpooli Ülikool ning seda rahastavad ühiselt Innovate UK, Meditsiiniuuringute Nõukogu (MRC), Ravimite ja Tervishoiutoodete Reguleerimisamet (MHRA) ja Eluteaduste Amet (OLS). Keskuse eesmärk on kiirendada farmakogenoomika (PGx) ohutut ja tõhusat integreerimist riiklikku tervishoiuteenistusse (NHS), kõrvaldades peamised rakendamise takistused. See juhend on esimene kliiniline juhend pärast CERSI PGx loomist.
Miks CYP2C19 on klopidogreeli puhul oluline?
CYP2C19 on tsütokroom P450 ensüümide perekonna võtmeelement, mis vastutab paljude ravimite metaboolse aktiveerimise või inaktiveerimise eest. CYP2C19 geneetilised polümorfismid põhjustavad ravimite metabolismis olulisi individuaalseid erinevusi, mis mõjutavad efektiivsust ja ohutust.
Klopidogreel on laialdaselt kasutatav trombotsüütidevastane aine trombootiliste sündmuste ennetamiseks koronaararterite haiguse, isheemilise insuldi, perifeersete arterite haiguse ja kodade virvenduse korral. Eelravimina vajab klopidogreel metaboolset aktivatsiooni CYP2C19 poolt. Juhendis liigitatakse inimesed CYP2C19 genotüübi põhjal ülikiireteks, kiireteks, normaalseteks, keskmisteks ja aeglasteks metaboliseerijateks. Funktsioonikaotuse alleelide (nt CYP2C192 ja *3*) kandjad – keskmiste ja aeglaste metaboliseerijate nimed – ei suuda klopidogreeli efektiivselt aktiveerida, mis viib ebapiisava trombotsüütide inhibeerimiseni ja suurenenud tromboosi korduva riskini.
CYP2C192 alleeli esinemissagedus on eurooplastel ligikaudu 15%, Lõuna-Aasia elanikel 30% ja Okeaania põlisrahvaste seas koguni 60%.
Peamine soovitus: Klopidogreeli CYP2C19 universaalne testimine
Juhendis on sätestatud, et olenemata näidustusest peaksid kõik patsiendid, kelle puhul klopidogreeli kasutamist kaalutakse, läbima ...CYP2C19genotüüpimine.Tulemuste põhjal tuleks trombotsüütidevastast ravi optimeerida:
-Aeglased metaboliseerijadpeaksid vältima klopidogreeli ja eelistama alternatiivseid ravimeid, mis ei sõltu CYP2C19 metabolismist, näiteks tikagreloori või prasugreeli.
-Keskmise kiirusega metaboliseerijadpeaksid kaaluma ka alternatiivseid ravimeid või kohandatud raviskeeme, mitte ainult klopidogreeli annuse suurendamist.
Ühendkuningriigis on klopidogreel heaks kiidetud aterotrombootiliste sündmuste sekundaarseks ennetamiseks, mõõduka kuni kõrge riskiga mööduva isheemilise ataki (TIA) või kerge isheemilise insuldi korral ning aterotrombootiliste ja trombemboolsete sündmuste ennetamiseks kodade virvenduse korral.
Lisaks klopidogreelile: muud ravimid, mille puhul CYP2C19 genotüüpimine on kriitilise tähtsusega
CYP2C19 genotüüpimise väärtus ulatub klopidogreelist kaugemale. Peamise ravimeid metaboliseeriva ensüümina mängib CYP2C19 olulist rolli ka vorikonasooli, mitmete antidepressantide ja prootonpumba inhibiitorite (PPI-de) metabolismis. Mitmed rahvusvahelised ja riiklikud juhised soovitavad nende ravimite puhul genotüübipõhist individualiseerimist.
1. Antidepressandid (SSRI-d)
Selektiivsed serotoniini tagasihaarde inhibiitorid (SSRI-d) – näiteks sertraliin, tsitalopraam ja estsitalopraam – on depressiooni esmavaliku ravimid ja neid metaboliseerib peamiselt CYP2C19. CYP2C19 ensüümi aktiivsus määrab otseselt nende ravimite plasmakontsentratsiooni. Aeglastel metaboliseerijatel on ravimi kliirens 30–60% vähenenud, mis soodustab kõrvaltoimeid, nagu QT-intervalli pikenemine ja sedatsioon. Ülikiiretel metaboliseerijatel on sageli subterapeutilised plasmakontsentratsioonid, mis viib ravivastuse hilinemiseni ja ravimi võtmise katkestamise riski suurenemiseni.
2023. aasta kliinilise farmakogeneetika rakendamise konsortsiumi (CPIC) suunises on sätestatud, et tsitalopraami või estsitalopraami võtvatel aeglastel metaboliseerijatel on suurenenud QT-intervalli pikenemise risk ja soovitatakse annust vähendada 50%. Hollandi farmakogeneetika töörühma (DPWG) 2021. aasta suunises soovitatakse, et aeglastel metaboliseerijatel tuleks saada estsitalopraami maksimaalset annust 50% võrra vähendatuna ja et ülikiired metaboliseerijad peaksid estsitalopraami täielikult vältima. Sertraliini puhul soovitab DPWG aeglastel metaboliseerijatel ööpäevast annust mitte ületada 75 mg.
Oluline on see, et hiljuti avaldatud Hiina psühhiaatrias farmakogenoomilise testimise ekspertide konsensus (2025), mille töötas välja Hiina Psühhiaatriaühingu täppismeditsiini koostöögrupp, sisaldab selgesõnalisi soovitusi CYP2C19 genotüüpimise kohta. Konsensusavalduses märgitakse, et Hiina populatsioonide puhul saab viidata rahvusvaheliste suuniste, näiteks CPIC ja DPWG, annuse kohandamise soovitustele ravimeid metaboliseerivate ensüümide (sealhulgas CYP2C19) kohta. Seetõttu võimaldab CYP2C19 genotüüpimine enne SSRI-ravi alustamist (nt estsitalopraam) optimeerida annust või minna üle alternatiivsetele ravimitele, mida CYP2C19 ei metaboliseeri, saavutades seeläbi täppisravi, parandades ravivastuse määra ja vähendades kõrvaltoimeid.
2. Prootonpumba inhibiitorid (PPI-d)
Prootonpumba inhibiitoreid – sealhulgas omeprasooli, lansoprasooli ja pantoprasooli – kasutatakse laialdaselt happega seotud häirete, näiteks gastroösofageaalse reflukshaiguse ja peptiliste haavandite korral. Nende metabolism sõltub samuti suuresti CYP2C19-st. Erineva CYP2C19 genotüübiga patsientidel on PPI-de suhtes märkimisväärselt varieeruv reaktsioon. Funktsioonikaotuse alleelide (*2, *3) kandjatel on märkimisväärselt suurenenud ravimi ekspositsioon, mis võib suurendada happe supressiooni, aga ka suurendada kõrvaltoimete riski. Seevastu normaalsetel metaboliseerijatel on plasmakontsentratsioon suhteliselt madalam ja nad võivad kogeda nõrgemat happe supressiooni, kuigi individuaalsed erinevused on endiselt märkimisväärsed.
2020. aasta CPIC-i PPI-de suunis soovitab, et ülikiired metaboliseerijad, kes võtavad omeprasooli või sarnaseid ravimeid, metaboliseeriksid ravimit liiga kiiresti, mille tulemuseks on ebapiisav plasmakontsentratsioon ja halb happe supressioon. Nendel patsientidel tuleks annust suurendada ja jälgida ravivastust. Aeglaste metaboliseerijate korral on ravimi kliirens aeglane ja plasmakontsentratsioon võib tõusta; kuigi efektiivsus võib olla parem, on ravimi toksilisuse potentsiaal suurem. Annuse vähendamine ja ravivastuse jälgimine on mõistlikud kaalutlused. Seetõttu on patsientidel, kes alustavad PPI-ravi või kellel esineb halb ravivastus või kõrvaltoimed, soovitatav CYP2C19 genotüüpimine, et suunata individuaalset annustamist, optimeerida efektiivsust ja minimeerida kõrvaltoimeid.
3. Vorikonasool
Vorikonasool on laia toimespektriga seenevastane aine, mida kasutatakse tõsiste seeninfektsioonide, näiteks invasiivse aspergilloosi raviks. Sellel on kitsas terapeutiline aken: liiga kõrge plasmakontsentratsioon suurendab maksatoksilisuse ja nägemishäirete riski, samas kui madal kontsentratsioon põhjustab ravi ebaõnnestumist. Vorikonasooli metabolismi vahendab peamiselt CYP2C19 ja geneetilised polümorfismid mõjutavad oluliselt selle plasmakontsentratsiooni.
CPIC avaldas 2016. aastal spetsiaalse CYP2C19 ja vorikonasooli kohta suunise. Selles on märgitud, et ülikiiretel metaboliseerijatel on vorikonasooli minimaalne kontsentratsioon madalam ja sageli ei saavutata sihttasemeid terapeutiliselt. Aeglastel metaboliseerijatel on minimaalne kontsentratsioon kõrgenenud ja kõrvaltoimete risk oluliselt suurenenud. CPIC suunis annab genotüübi põhjal spetsiifilised annustamissoovitused. Näiteks peaksid täiskasvanud ülikiired metaboliseerijad saama alternatiivseid esmavaliku ravimeid, mis ei sõltu CYP2C19 metabolismist, näiteks isavukonasool, liposomaalne amfoteritsiin B või posakonasool. Seetõttu võimaldab CYP2C19 genotüüpimine enne vorikonasoolravi individuaalset annustamist ja vähendab ravimiga seotud kõrvaltoimete esinemissagedust.
Kliiniline tähtsus: ravimite usaldusväärsemaks muutmine
Äsja avaldatud juhis asetab CYP2C19 genotüüpimise taas täppismeditsiini esirinnas esiplaanile. Siiski on oluline mõista, et CYP2C19 genotüüpimise kliinilised rakendused ulatuvad klopidogreelist palju kaugemale – alates vorikonasoolist (seenevastane ravim) ja SSRI-dest (antidepressandid) kuni prootonpumba inhibiitoriteni happe supressiooniks. CYP2C19 genotüüp toimib ravimteraapia „kompassina“.
Täppismeditsiini laiema aktsepteerimise tõttu kaasab üha rohkem autoriteetseid suuniseid CYP2C19 genotüüpimise tavapärastesse ravimite töövoogudesse. Patsientide jaoks aitab oma CYP2C19 genotüübi tundmine mõista oma individuaalset ravimireaktsiooni profiili ja võimaldab teha koos arstiga ühiseid otsuseid sobivama raviplaani väljatöötamiseks. Arstide jaoks on objektiivsete geneetiliste testide tulemuste integreerimine väljakirjutamisotsustesse võimas vahend ravi kvaliteedi parandamiseks ja patsiendi ohutuse tagamiseks.
Makro- ja mikrotestid'sCYP2C19 genotüpiseerimise lahus
Macro & Micro Test pakub CYP2C19 genotüüpimise komplekti, mis põhineb täiustatud amplifikatsiooni refraktaarse mutatsiooni süsteemil (ARMS) koos Taqmani sondidega ning millel on järgmised omadused:
-Põhjalik alleelide katvus– tuvastabCYP2C192, *3 ja *17ilma oluliste variantideta.
-Tugev kvaliteedikontroll– sisaldab negatiivseid/positiivseid kontrolle, sisemist kontrolli ja UDG ensüümi neljatasandiliseks kvaliteedikontrolliks täpsete tulemuste tagamiseks.
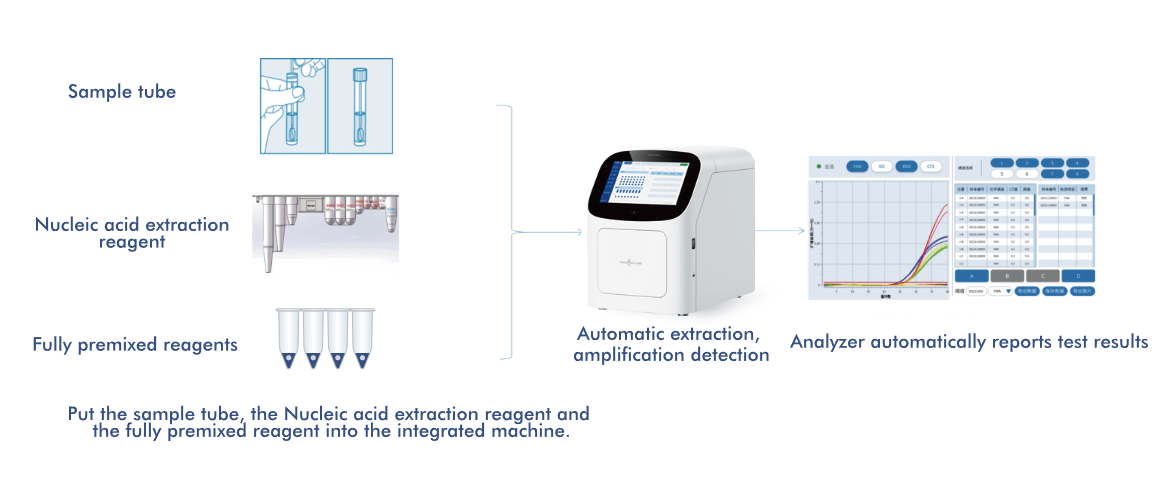
-Automatiseeritud ekstraheerimine– ühildub Macro & Micro-Testi täisautomaatse nukleiinhapete ekstraktoriga, parandades töövoo tõhusust.
-Lai ühilduvus– töötab turul saadaolevate tavaliste reaalaja PCR-instrumentidega, sh ABI 7500 Hongshi SLAN 96P-ga.
-Automatiseeritud tulemuste tõlgendamine– spetsiaalne analüüsitarkvara (seadmetel ABI 7500, SLAN 96P jne) võimaldab tulemuste automaatset tõlgendamist, suurendades tõhusust.
-POCT-valmis automatiseerimine– HWTS AIO800 täisautomaatne nukleiinhapete amplifikatsioonianalüsaator võimaldab „proov sisse, tulemus välja“ toimimist.
Farmakogenoomika pideva arenguga kaasneb eeldatavasti CYP2C19 genotüüpimise kasu üha suuremale hulgale patsientidele, nihutades täppismeditsiini kontseptsioonist rutiinsesse kliinilisse praktikasse. Äsja avaldatud CERSI PGx juhend kinnitab CYP2C19 testimise kriitilist rolli mitte ainult klopidogreeli, vaid ka üha kasvava ravimite nimekirja, sealhulgas antidepressantide, prootonpumba inhibiitorite ja vorikonasooli puhul. Genotüübipõhise väljakirjutamise laialdase kasutuselevõtu hõlbustamiseks on hädavajalikud usaldusväärsed ja kasutajasõbralikud testimislahendused. Macro & Micro-Testi farmakogenoomilise testimise portfell, mis hõlmab ulatuslikku alleelide katvust, tugevat kvaliteedikontrolli ja automatiseerimisvalmis platvorme, on suunatud tervishoiuteenuse osutajate toetamisele täppismeditsiini rakendamisel ja lõppkokkuvõttes patsientide tervise kaitsmisel.
Seotud tooted:
Viited:
1. Lima JJ, Thomas CD, Barbarino J jt. Kliinilise farmakogeneetika rakendamise konsortsiumi (CPIC) CYP2C19 ja prootonpumba inhibiitorite annustamise juhend. Clin Pharmacol Ther. 2020. doi:10.1002/cpt.20151.
2. Lee CR, Luzum JA, Sangkuhl K jt. Kliinilise farmakogeneetika rakendamise konsortsiumi juhend CYP2C19 genotüübi ja klopidogreeliravi kohta: 2022. aasta uuendus. Clin Pharmacol Ther. 2022. doi:10.1002/cpt.25261.
3. Riiklik Tervise ja Hoolduse Tippkeskus (NICE). CYP2C19 genotüübi testimine klopidogreeli kasutamise suunamiseks pärast isheemilist insulti või mööduvat isheemilist atakki. Diagnostiline juhend DG59. Avaldatud: 31. juuli 2024.
4. Hiina Psühhiaatriaühingu täppismeditsiini uuringute koostöörühm. Ekspertide konsensus farmakogenoomilise testimise kohta psühhiaatrias (2025) [Zhonghua Jing Shen Ke Za Zhi].Hiina psühhiaatria ajakiri. 2025;58(6):434-445. doi:10.3760/cma.j.cn11366120240611-00181
5. Dello Russo C, Frater I, Kuruvilla R jt. CYP2C19 genotüübi testimine klopidogreeli suhtes: Ühendkuningriigi farmakogenoomika regulatiivse teaduse ja innovatsiooni tippkeskuse (CERSI-PGx) väljatöötatud juhend. Br J Clin Pharmacol. 2025. DOI: 10.1093/bjcp/…
6. Moriyama B, Owusu Obeng A, Barbarino J jt. Kliinilise farmakogeneetika rakendamise konsortsiumi (CPIC) juhised CYP2C19 ja vorikonasooli ravi kohta. Clin Pharmacol Ther. 2017;102(1):45-51. doi:10.1002/cpt.595.
7. Bousman CA, Stevenson JM, Ramsey LB jt. Kliinilise farmakogeneetika rakendamise konsortsiumi (CPIC) juhend CYP2D6, CYP2C19, CYP2B6, SLC6A4 ja HTR2A genotüüpide ning serotoniini tagasihaarde inhibiitorite antidepressantide kohta. Clin Pharmacol Ther. 2023;114(1):51-68. doi:10.1002/cpt.2903.
8. Brouwer JMJL, Nijenhuis M, Soree B jt. Hollandi Farmakogeneetika Töörühma (DPWG) juhised CYP2C19 ja CYP2D6 ning SSRI-de vahelise geeni ja ravimi koostoime kohta. Eur J Hum Genet. 2021. doi:10.1038/s41431-021-00894-2.
Postituse aeg: 22. aprill 2026